1. ចំណេះដឹងជាមូលដ្ឋាន (ប្រសិនបើអ្នកចង់ឃើញផ្នែកពិសោធន៍ សូមផ្ទេរដោយផ្ទាល់ទៅផ្នែកទីពីរ)
ជាប្រតិកម្មដេរីវេនៃ PCR ធម្មតា ពេលវេលាពិត PCR ត្រួតពិនិត្យជាចម្បងលើការផ្លាស់ប្តូរបរិមាណនៃផលិតផល amplification នៅក្នុងវដ្តនីមួយៗនៃប្រតិកម្ម PCR amplification ក្នុងពេលវេលាជាក់ស្តែងតាមរយៈការផ្លាស់ប្តូរនៃសញ្ញា fluorescence និងវិភាគបរិមាណនៃគំរូចាប់ផ្តើមតាមរយៈទំនាក់ទំនងរវាងតម្លៃ ct និងខ្សែកោងស្តង់ដារ។
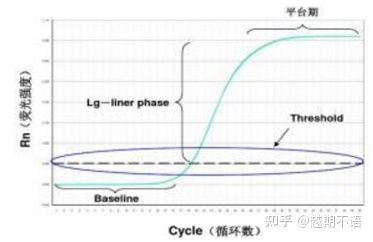
ទិន្នន័យជាក់លាក់នៃ RT-PCR គឺបន្ទាត់មូលដ្ឋាន, កម្រិត fluorescenceនិងតម្លៃ Ct ។
| បន្ទាត់មូលដ្ឋាន៖ | តម្លៃ fluorescence នៃវដ្តទី 3-15 គឺជាបន្ទាត់មូលដ្ឋាន (បន្ទាត់មូលដ្ឋាន) ដែលបណ្តាលមកពីកំហុសម្តងម្កាលនៃការវាស់វែង។ |
| កម្រិត (កម្រិត)៖ | សំដៅទៅលើដែនកំណត់នៃការរកឃើញ fluorescence ដែលបានកំណត់នៅទីតាំងសមស្របមួយនៅក្នុងតំបន់កំណើនអិចស្ប៉ូណង់ស្យែលនៃខ្សែកោងពង្រីក ជាទូទៅ 10 ដងនៃគម្លាតស្តង់ដារនៃបន្ទាត់មូលដ្ឋាន។ |
| តម្លៃ CT៖ | វាគឺជាចំនួននៃវដ្ត PCR នៅពេលដែលតម្លៃ fluorescence នៅក្នុងបំពង់ប្រតិកម្មនីមួយៗឈានដល់កម្រិត។ តម្លៃ Ct គឺសមាមាត្រច្រាសទៅនឹងបរិមាណនៃគំរូដំបូង។ |
វិធីសាស្ត្រដាក់ស្លាកទូទៅសម្រាប់ RT-PCR៖
| វិធីសាស្រ្ត | អត្ថប្រយោជន៍ | កង្វះខាត | វិសាលភាពនៃកម្មវិធី |
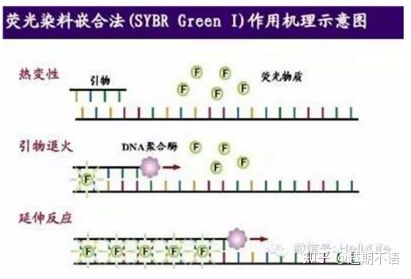
| SYBR GreenⅠ | ការអនុវត្តយ៉ាងទូលំទូលាយ រសើប ថោក និងងាយស្រួល | តម្រូវការ primer គឺខ្ពស់ ងាយនឹងក្រុមតន្រ្តីមិនជាក់លាក់ | វាស័ក្តិសមសម្រាប់ការវិភាគបរិមាណនៃហ្សែនគោលដៅផ្សេងៗ ការស្រាវជ្រាវលើការបញ្ចេញហ្សែន និងការស្រាវជ្រាវលើសត្វ និងរុក្ខជាតិដែលផ្លាស់ប្តូរហ្សែន។ |
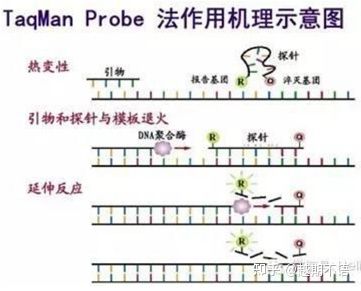
| តាកម៉ាន់ | ភាពជាក់លាក់ល្អ និងអាចធ្វើម្តងទៀតបានខ្ពស់។ | តម្លៃគឺខ្ពស់ ហើយសមរម្យសម្រាប់តែគោលដៅជាក់លាក់ប៉ុណ្ណោះ។ | ការរកឃើញធាតុបង្កជំងឺ ការស្រាវជ្រាវហ្សែនធន់នឹងថ្នាំ ការវាយតម្លៃប្រសិទ្ធភាពថ្នាំ ការធ្វើរោគវិនិច្ឆ័យជំងឺហ្សែន។ |
| សញ្ញាម៉ូលេគុល | ភាពជាក់លាក់ខ្ពស់ fluorescence ផ្ទៃខាងក្រោយទាប | តម្លៃគឺខ្ពស់វាសមរម្យសម្រាប់តែគោលបំណងជាក់លាក់ការរចនាពិបាកហើយតម្លៃក៏ខ្ពស់។ | ការវិភាគហ្សែនជាក់លាក់ ការវិភាគ SNP |
2. ជំហានពិសោធន៍
2.1 អំពីក្រុមពិសោធន៍- ត្រូវតែមានអណ្តូងជាច្រើននៅក្នុងក្រុម ហើយត្រូវតែមានពាក្យដដែលៗជីវសាស្រ្ត។
| ① | ការគ្រប់គ្រងទទេ | ប្រើដើម្បីរកមើលស្ថានភាពលូតលាស់កោសិកានៅក្នុងការពិសោធន៍ |
| ② | ការត្រួតពិនិត្យអវិជ្ជមាន siRNA (លំដាប់ siRNA មិនជាក់លាក់) | បង្ហាញពីភាពជាក់លាក់នៃសកម្មភាព RNAi ។siRNA អាចបង្កើតការឆ្លើយតបស្ត្រេសមិនជាក់លាក់នៅកំហាប់ 200nM ។ |
| ③ | ការគ្រប់គ្រងសារធាតុចម្លង | មិនរាប់បញ្ចូលការពុលនៃសារធាតុចម្លងទៅកោសិកា ឬឥទ្ធិពលលើការបញ្ចេញហ្សែនគោលដៅ |
| ④ | siRNA ប្រឆាំងនឹងហ្សែនគោលដៅ | ទម្លាក់ការបញ្ចេញមតិនៃហ្សែនគោលដៅ |
| ⑤ (ជាជម្រើស) | siRNA វិជ្ជមាន | ប្រើដើម្បីដោះស្រាយបញ្ហាប្រព័ន្ធពិសោធន៍ និងបញ្ហាប្រតិបត្តិការ |
| ⑥ (ស្រេចចិត្ត) | ការត្រួតពិនិត្យ fluorescent siRNA | ប្រសិទ្ធភាពនៃការចម្លងកោសិកាអាចត្រូវបានគេសង្កេតឃើញដោយប្រើមីក្រូទស្សន៍ |
2.2 គោលការណ៍នៃការរចនាបឋម
| ពង្រីកទំហំបំណែក | និយមនៅ 100-150bp |
| ប្រវែង primer | 18-25bp |
| មាតិកា GC | 30%-70%, និយម 45%-55% |
| តម្លៃ Tm | 58-60 ℃ |
| លំដាប់ | ជៀសវាង T/C បន្ត;A/G បន្ត |
| លំដាប់ទី ៣ | ជៀសវាង GC rich ឬ AT rich;មូលដ្ឋានស្ថានីយគឺល្អ G ឬ C;វាជាការល្អបំផុតដើម្បីជៀសវាង T |
| ការបំពេញបន្ថែម | ជៀសវាងការបំពេញបន្ថែមនៃមូលដ្ឋានលើសពី 3 នៅក្នុង primer ឬរវាង primers ពីរ |
| ភាពជាក់លាក់ | ប្រើការស្វែងរកការផ្ទុះដើម្បីបញ្ជាក់ភាពជាក់លាក់នៃ primer |
①SiRNA គឺជាប្រភេទសត្វជាក់លាក់ ហើយលំដាប់នៃប្រភេទផ្សេងៗគ្នានឹងខុសគ្នា។
②SiRNA ត្រូវបានខ្ចប់ជាម្សៅស្ងួត ដែលអាចរក្សាទុកបានយ៉ាងឋិតថេររយៈពេល 2-4 សប្តាហ៍នៅសីតុណ្ហភាពបន្ទប់។
2.3 ឧបករណ៍ឬសារធាតុដែលចាំបាច់ត្រូវរៀបចំជាមុន
| Primer (ឯកសារយោងខាងក្នុង) | រួមទាំងទៅមុខ និងបញ្ច្រាសពីរ |
| Primers (ហ្សែនគោលដៅ) | រួមទាំងទៅមុខ និងបញ្ច្រាសពីរ |
| គោលដៅ Si RNA (3 បន្ទះ) | ជាទូទៅក្រុមហ៊ុននឹងសំយោគបន្ទះចំនួន 3 ហើយបន្ទាប់មកជ្រើសរើសមួយក្នុងចំណោមបីដោយ RT-PCR |
| កញ្ចប់ផ្ទេរ | Lipo2000 ជាដើម។ |
| កញ្ចប់ទាញយករហ័ស RNA | សម្រាប់ការទាញយក RNA បន្ទាប់ពីការផ្ទេរ |
| កញ្ចប់ប្រតិចារិកបញ្ច្រាសរហ័ស | សម្រាប់ការសំយោគ cDNA |
| កញ្ចប់ពង្រីក PCR | 2 × Super SYBR បៃតង qPCR Master Mix |
2.4 ទាក់ទងនឹងបញ្ហាដែលត្រូវយកចិត្តទុកដាក់ក្នុងជំហានពិសោធន៍ជាក់លាក់៖
① ដំណើរការផ្ទេរ siRNA
1. សម្រាប់ការដាក់ចាន អ្នកអាចជ្រើសរើសចាន 24 អណ្តូង ចាន 12 អណ្តូង ឬចាន 6 អណ្តូង (កំហាប់ RNA ជាមធ្យមដែលបានស្នើឡើងក្នុងអណ្តូងនីមួយៗនៃ 24 អណ្តូងគឺប្រហែល 100-300 ng/uL) ហើយដង់ស៊ីតេនៃការបញ្ជូនល្អបំផុតនៃកោសិកាគឺរហូតដល់ 60%-80% ឬដូច្នេះ។
2. ជំហាននៃការឆ្លង និងតម្រូវការជាក់លាក់គឺយ៉ាងតឹងរ៉ឹងស្របតាមការណែនាំ។
3. បន្ទាប់ពីការចម្លង គំរូអាចត្រូវបានប្រមូលក្នុងរយៈពេល 24-72 ម៉ោងសម្រាប់ការរកឃើញ mRNA (RT-PCR) ឬការរកឃើញប្រូតេអ៊ីនក្នុងរយៈពេល 48-96 ម៉ោង (WB)
② ដំណើរការទាញយក RNA
1. ការពារការចម្លងរោគដោយអង់ស៊ីម exogenous ។វារួមបញ្ចូលទាំងការពាក់ម៉ាស់ និងស្រោមដៃយ៉ាងតឹងរ៉ឹង។ដោយប្រើគន្លឹះបំពង់មាប់មគ និងបំពង់ EP;ទឹកដែលប្រើក្នុងការពិសោធន៍ត្រូវតែជា RNase-Free។
2. វាត្រូវបានផ្ដល់អនុសាសន៍ឱ្យធ្វើពីរដងដូចដែលបានណែនាំនៅក្នុងឧបករណ៍ទាញយករហ័ស ដែលពិតជានឹងធ្វើអោយប្រសើរឡើងនូវភាពបរិសុទ្ធ និងទិន្នផល។
3. សារធាតុរាវកាកសំណល់មិនត្រូវប៉ះជួរឈរ RNA ។
③ បរិមាណ RNA
បន្ទាប់ពី RNA ត្រូវបានស្រង់ចេញ វាអាចត្រូវបានកំណត់បរិមាណដោយផ្ទាល់ជាមួយ Nanodrop ហើយការអានអប្បបរមាអាចទាបរហូតដល់ 10ng/ul។
④ ដំណើរការចម្លងបញ្ច្រាស
1. ដោយសារតែភាពប្រែប្រួលខ្ពស់នៃ RT-qPCR យ៉ាងហោចណាស់អណ្តូងប៉ារ៉ាឡែល 3 គួរតែត្រូវបានបង្កើតឡើងសម្រាប់គំរូនីមួយៗ ដើម្បីការពារ Ct ជាបន្តបន្ទាប់ពីភាពខុសគ្នាខ្លាំងពេក ឬ SD មានទំហំធំពេកសម្រាប់ការវិភាគស្ថិតិ។
2. កុំបង្កកនិងរលាយ Master លាយម្តងហើយម្តងទៀត។
3. បំពង់/រន្ធនីមួយៗត្រូវតែត្រូវបានជំនួសដោយព័ត៌មានជំនួយថ្មី!កុំបន្តប្រើចុងបំពង់ដូចគ្នា ដើម្បីបន្ថែមគំរូ!
4. ខ្សែភាពយន្តដែលភ្ជាប់ទៅនឹងចានអណ្តូង 96 បន្ទាប់ពីបន្ថែមគំរូចាំបាច់ត្រូវធ្វើឱ្យរលោងជាមួយនឹងចាន។វាជាការល្អបំផុតក្នុងការដាក់ centrifuge មុនពេលដាក់វានៅលើម៉ាស៊ីន ដើម្បីឱ្យវត្ថុរាវនៅលើជញ្ជាំងបំពង់អាចហូរចុះក្រោម និងយកពពុះខ្យល់ចេញ។
⑤ ការវិភាគខ្សែកោងទូទៅ
| គ្មានរយៈពេលនៃកំណើនលោការីត | ប្រហែលជាកំហាប់ខ្ពស់នៃគំរូ |
| គ្មានតម្លៃ CT | ជំហានមិនត្រឹមត្រូវសម្រាប់ការរកឃើញសញ្ញា fluorescent; ការរិចរិលនៃ primers ឬ probes - ភាពសុចរិតរបស់វាអាចត្រូវបានរកឃើញដោយ PAGE electrophoresis; ចំនួនមិនគ្រប់គ្រាន់នៃគំរូ; ការរិចរិលនៃគំរូ - ជៀសវាងការដាក់វត្ថុមិនបរិសុទ្ធ និងការកកម្តងហើយម្តងទៀត និងការរលាយក្នុងការរៀបចំគំរូ។ |
| Ct>៣៨ | ប្រសិទ្ធភាពពង្រីកទាប;ផលិតផល PCR វែងពេក;សមាសធាតុប្រតិកម្មផ្សេងៗត្រូវបានបំផ្លាញ |
| ខ្សែកោងពង្រីកលីនេអ៊ែរ | ការស៊ើបអង្កេតអាចត្រូវបានបំផ្លាញដោយផ្នែកដោយវដ្តនៃការកកម្តងហើយម្តងទៀតឬការប៉ះពាល់នឹងពន្លឺយូរ។ |
| ភាពខុសគ្នានៃរន្ធស្ទួនគឺមានទំហំធំជាពិសេស | ដំណោះស្រាយប្រតិកម្មមិនត្រូវបានរលាយទាំងស្រុងឬដំណោះស្រាយប្រតិកម្មមិនត្រូវបានលាយបញ្ចូលគ្នា;ការងូតទឹកកំដៅនៃឧបករណ៍ PCR ត្រូវបានបំពុលដោយសារធាតុ fluorescent |
2.5 អំពីការវិភាគទិន្នន័យ
ការវិភាគទិន្នន័យរបស់ qPCR អាចត្រូវបានបែងចែកជាបរិមាណទាក់ទង និងបរិមាណដាច់ខាត។ជាឧទាហរណ៍ កោសិកាក្នុងក្រុមព្យាបាល ប្រៀបធៀបជាមួយកោសិកាក្នុងក្រុមត្រួតពិនិត្យ
តើ mRNA នៃហ្សែន X ផ្លាស់ប្តូរប៉ុន្មានដង នេះគឺជាបរិមាណទាក់ទង។នៅក្នុងចំនួនជាក់លាក់នៃកោសិកា mRNA នៃហ្សែន X
តើមានច្បាប់ចម្លងចំនួនប៉ុន្មាន នេះជាបរិមាណដាច់ខាត។ជាធម្មតាអ្វីដែលយើងប្រើច្រើនបំផុតនៅក្នុងមន្ទីរពិសោធន៍គឺវិធីសាស្ត្របរិមាណទាក់ទង។ជាធម្មតាវិធីសាស្រ្ត 2-ΔΔctត្រូវបានគេប្រើច្រើនបំផុតក្នុងការពិសោធន៍ ដូច្នេះមានតែវិធីសាស្ត្រនេះប៉ុណ្ណោះដែលត្រូវបានណែនាំឱ្យបានលម្អិតនៅទីនេះ។
វិធីសាស្រ្ត 2-ΔΔct: លទ្ធផលដែលទទួលបានគឺភាពខុសគ្នានៃការបញ្ចេញហ្សែនគោលដៅនៅក្នុងក្រុមពិសោធន៍ទាក់ទងទៅនឹងហ្សែនគោលដៅនៅក្នុងក្រុមត្រួតពិនិត្យ។វាត្រូវបានទាមទារថា ប្រសិទ្ធភាពពង្រីកនៃទាំងហ្សែនគោលដៅ និងហ្សែនយោងខាងក្នុងគឺជិតដល់ 100% ហើយគម្លាតដែលទាក់ទងមិនគួរលើសពី 5% ទេ។
វិធីសាស្ត្រគណនាមានដូចខាងក្រោម៖
ក្រុមត្រួតពិនិត្យ Δct = តម្លៃ ct នៃហ្សែនគោលដៅនៅក្នុងក្រុមត្រួតពិនិត្យ - តម្លៃ ct នៃហ្សែនយោងខាងក្នុងនៅក្នុងក្រុមត្រួតពិនិត្យ
ក្រុមពិសោធន៍ Δct = តម្លៃ ct នៃហ្សែនគោលដៅក្នុងក្រុមពិសោធន៍ - តម្លៃ ct នៃហ្សែនយោងខាងក្នុងនៅក្នុងក្រុមពិសោធន៍
ΔΔct=Δct ក្រុមពិសោធន៍-Δct ក្រុមត្រួតពិនិត្យ
ជាចុងក្រោយ គណនាពហុគុណនៃភាពខុសគ្នាក្នុងកម្រិតកន្សោម៖
ផ្លាស់ប្តូរ Fold = 2-ΔΔct (ដែលត្រូវគ្នានឹងមុខងារ excel គឺ POWER)
ផលិតផលដែលពាក់ព័ន្ធ៖
ពេលវេលាផ្សាយ៖ ឧសភា-២០-២០២៣